Les personnages présentés sont de vrais patients et le consentement requis pour utiliser leurs histoires a été obtenu auprès des patients et de leurs familles. Les photographies sont à titre d'illustration uniquement.
Signes et symptômes
Chaque enfant peut ressentir différemment les symptômes, et la maladie est divisée selon différents types, en fonction de l’âge d’apparition de la maladie et en fonction de la capacité fonctionnelle. Il existe également des degrés de gravité dans chaque type, et jusqu’à 25 % des individus peuvent ne pas avoir de type précis.3
Caractéristiques de l’amyotrophie spinale
Cliquez sur les onglets afin d'obtenir les détails supplémentaires sur chaque type de SMA.
Progrès moteur le plus avancé
POSITION ASSISE IMPOSSIBLE
(« patients incapables de s’asseoir »)
Espérance de vie
≤ 2 ANS4
Type
Type I
(également appelé maladie de Werdnig-Hoffmann)
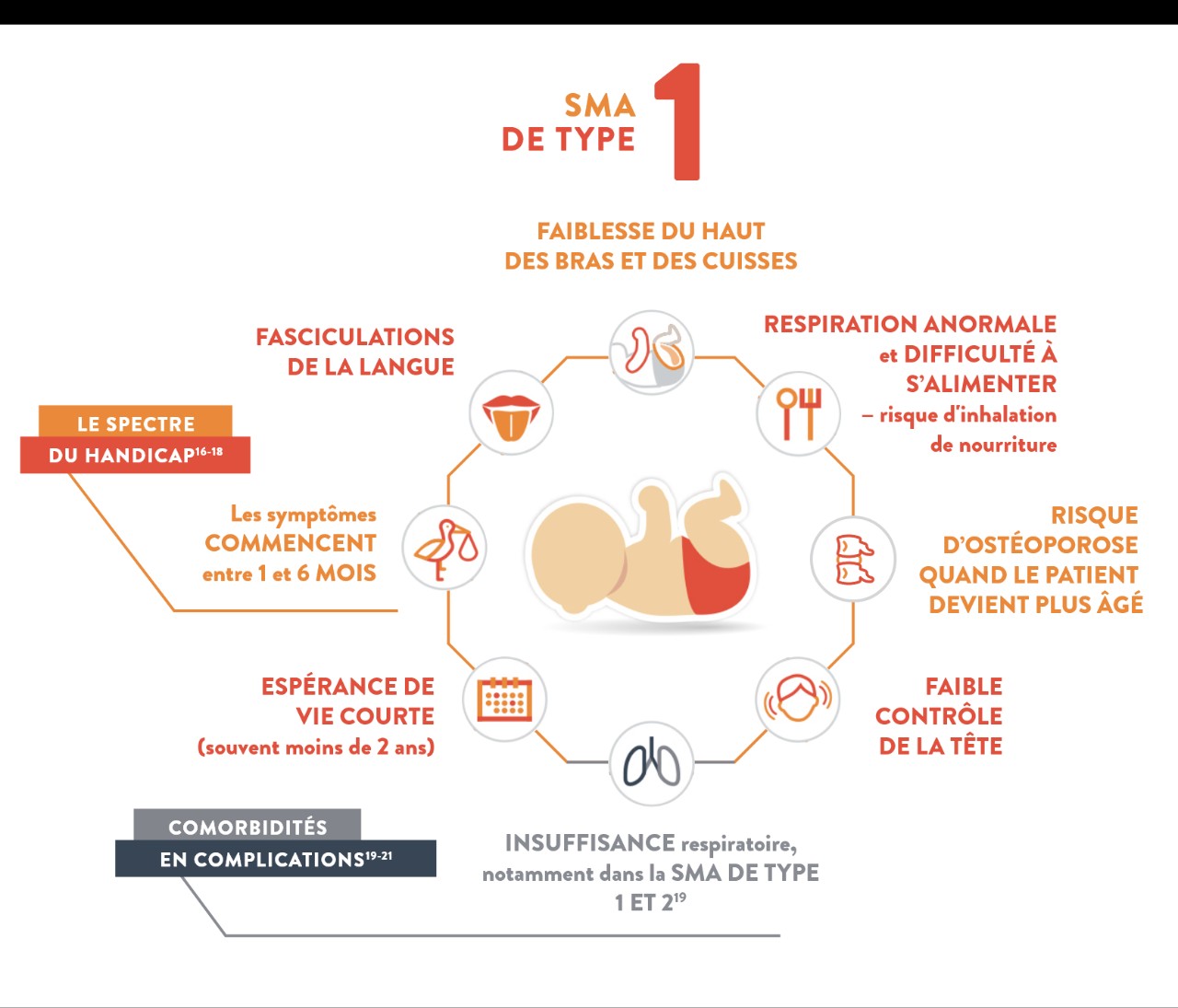
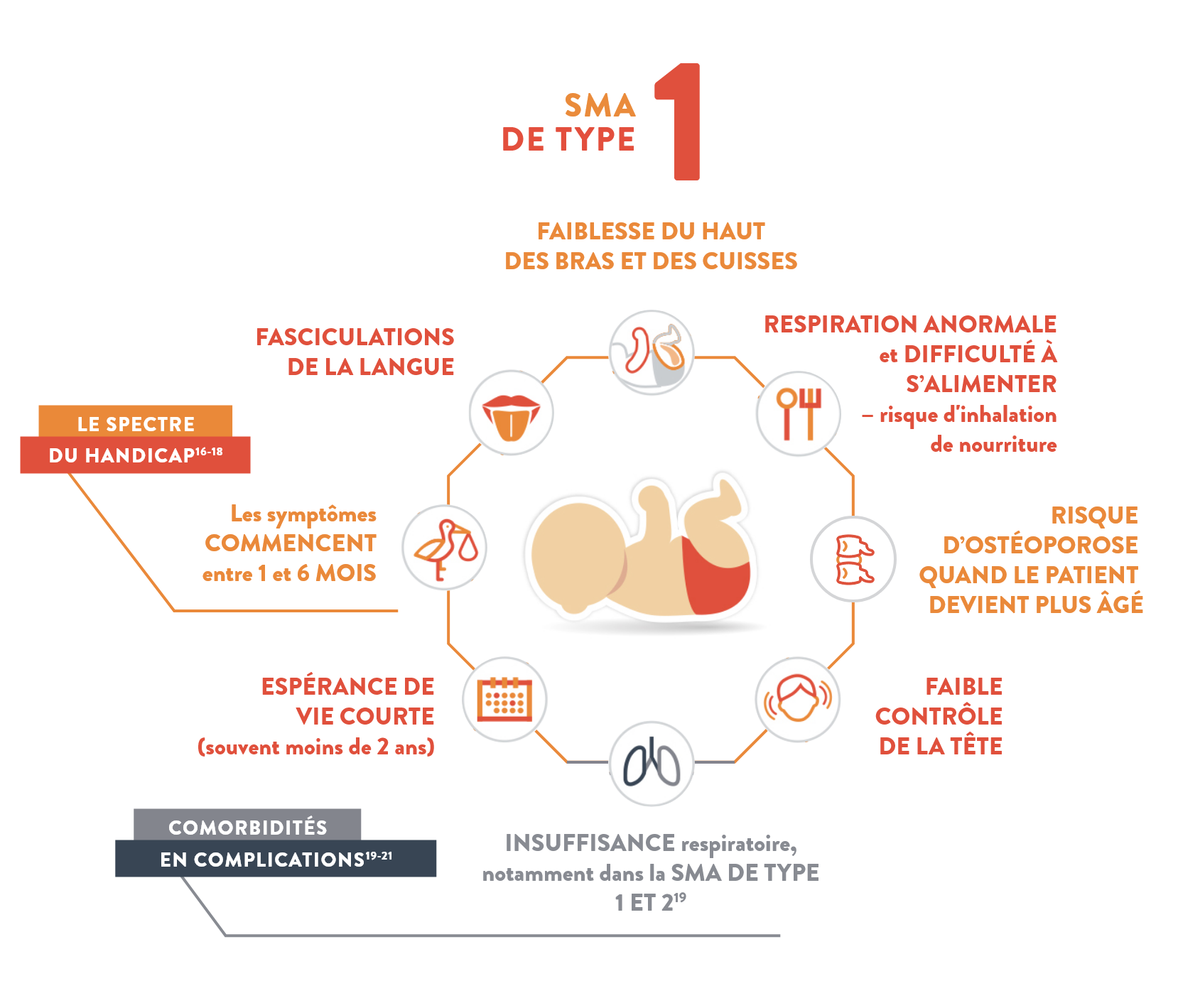
Caractéristiques1,4,5-7
- Faible contrôle de la tête
- Toux faible
- Larmoiement faible
- Affaiblissement progressif des muscles sollicités par la mastication et la déglutition
- Faible tonus musculaire
- « Position de la grenouille » en position allongée
- Faiblesse musculaire sévère des deux côtés du corps
- Faiblesse progressive des muscles qui aident à respirer (muscles intercostaux), entraînant la forme caractéristique « en cloche » du thorax
- Risque d'osthéoporose quand le patient devient plus âgé
Progrès moteur le plus avancé
POSITION ASSISE SANS SOUTIEN
(« patients capables de s’asseoir »)
Espérance de vie
> 2 ANS
70 % D’ENTRE EUX SONT ENCORE VIVANTS À L’ÂGE DE 25 ANS
Type
Type II
(également appelé syndrome de Dubowitz)
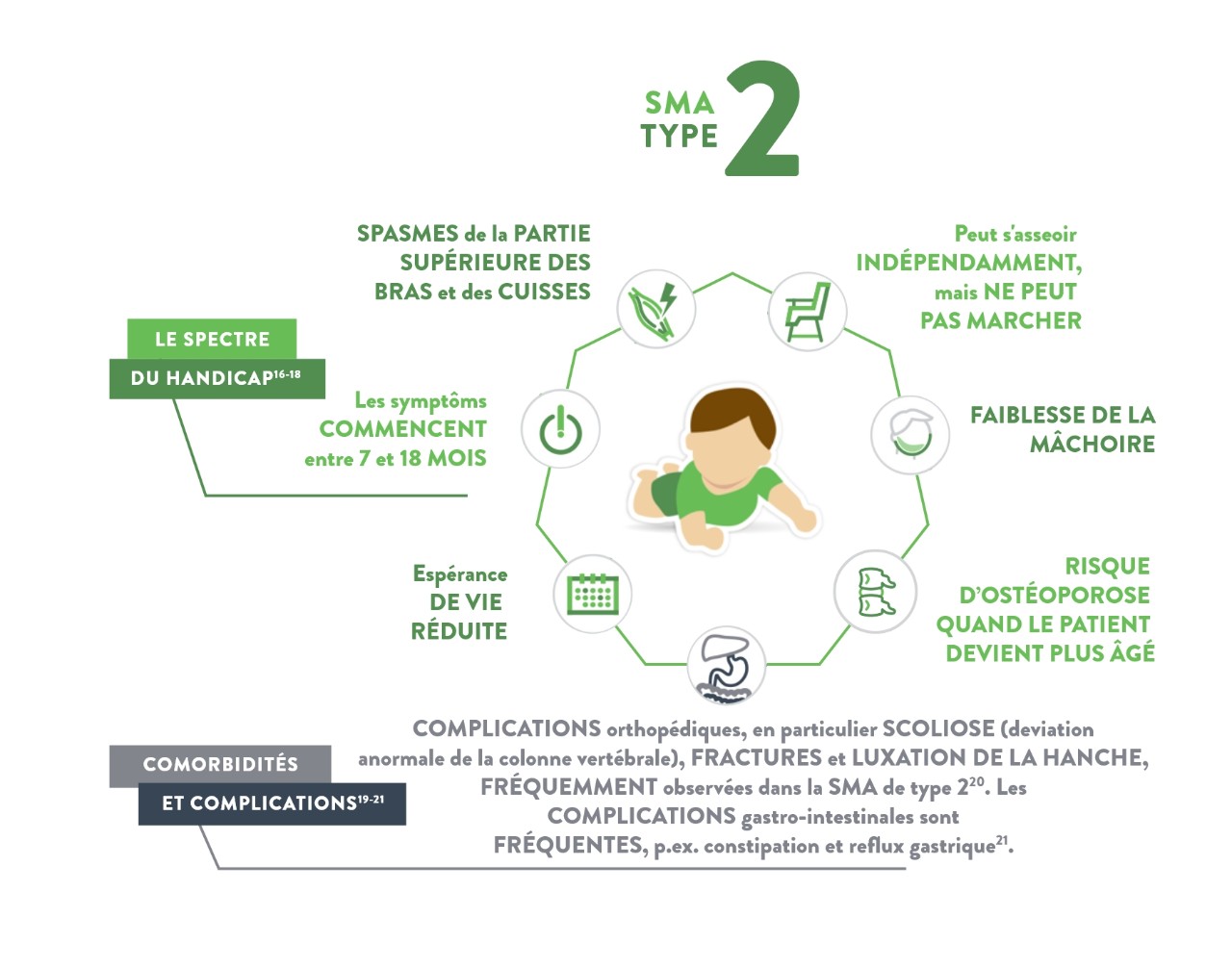
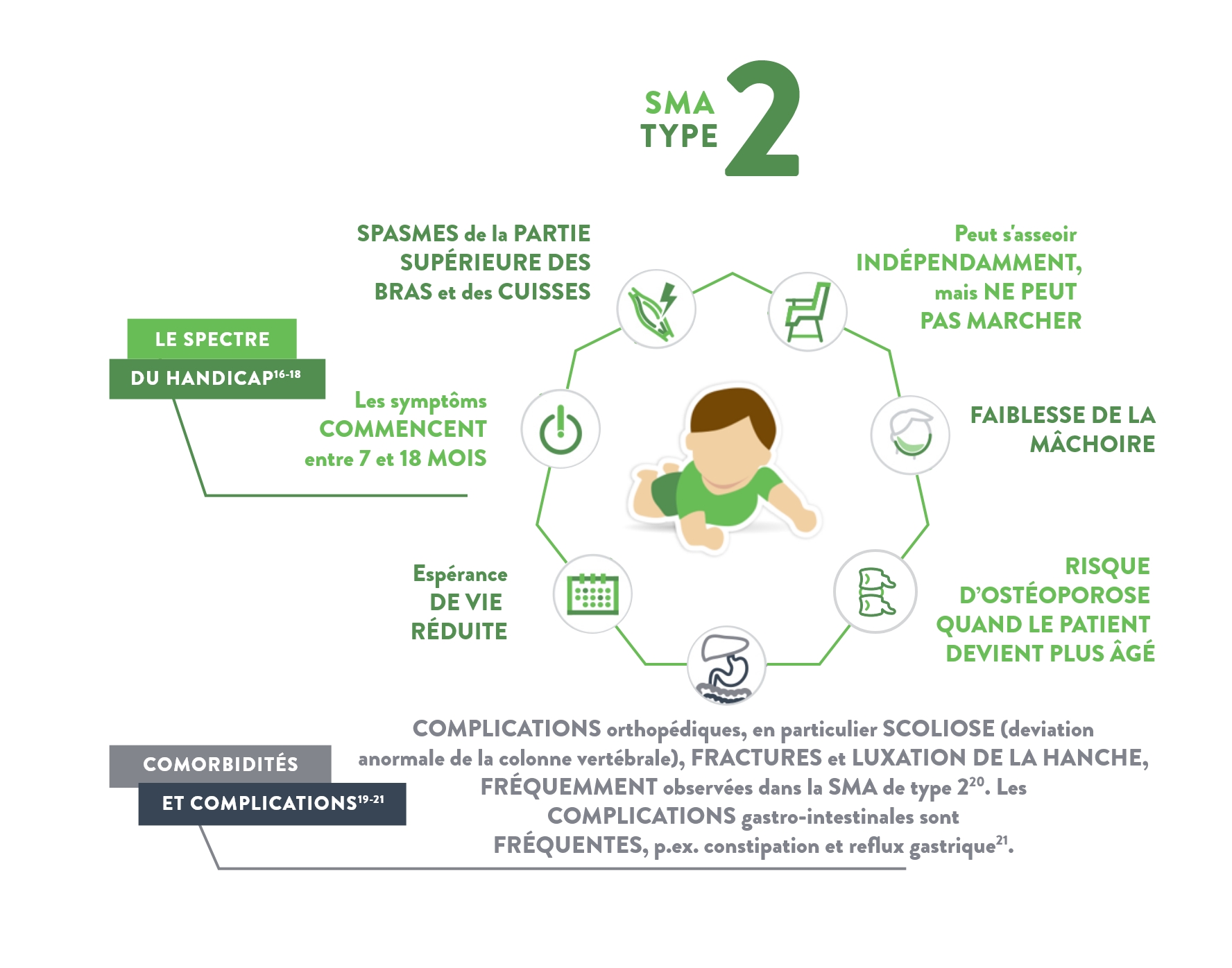
Caractéristiques1,5
- Faiblesse musculaire
- Les problèmes de déglutition, de toux et de respiration sont fréquents lorsque ces patients vieillissent
- Symptômes de douleurs musculaires et de raideurs articulaires
- La plupart des enfants atteints du type 2 développent des problèmes vertébraux tels qu’une scoliose (déviation de la colonne vertébrale), qui peut nécessiter une brassière de renfort ou une intervention chirurgicale
- Risque d'osthéoporose quand le patient devient plus âgé
Progrès moteur le plus avancé
CAPABLE DE MARCHER SEUL(E)
(« marcheurs », même s’ils peuvent progressivement perdre cette capacité)
Espérance de vie
NORMALE
Type
Type III
(également appelé maladie de Kugelberg-Welander)
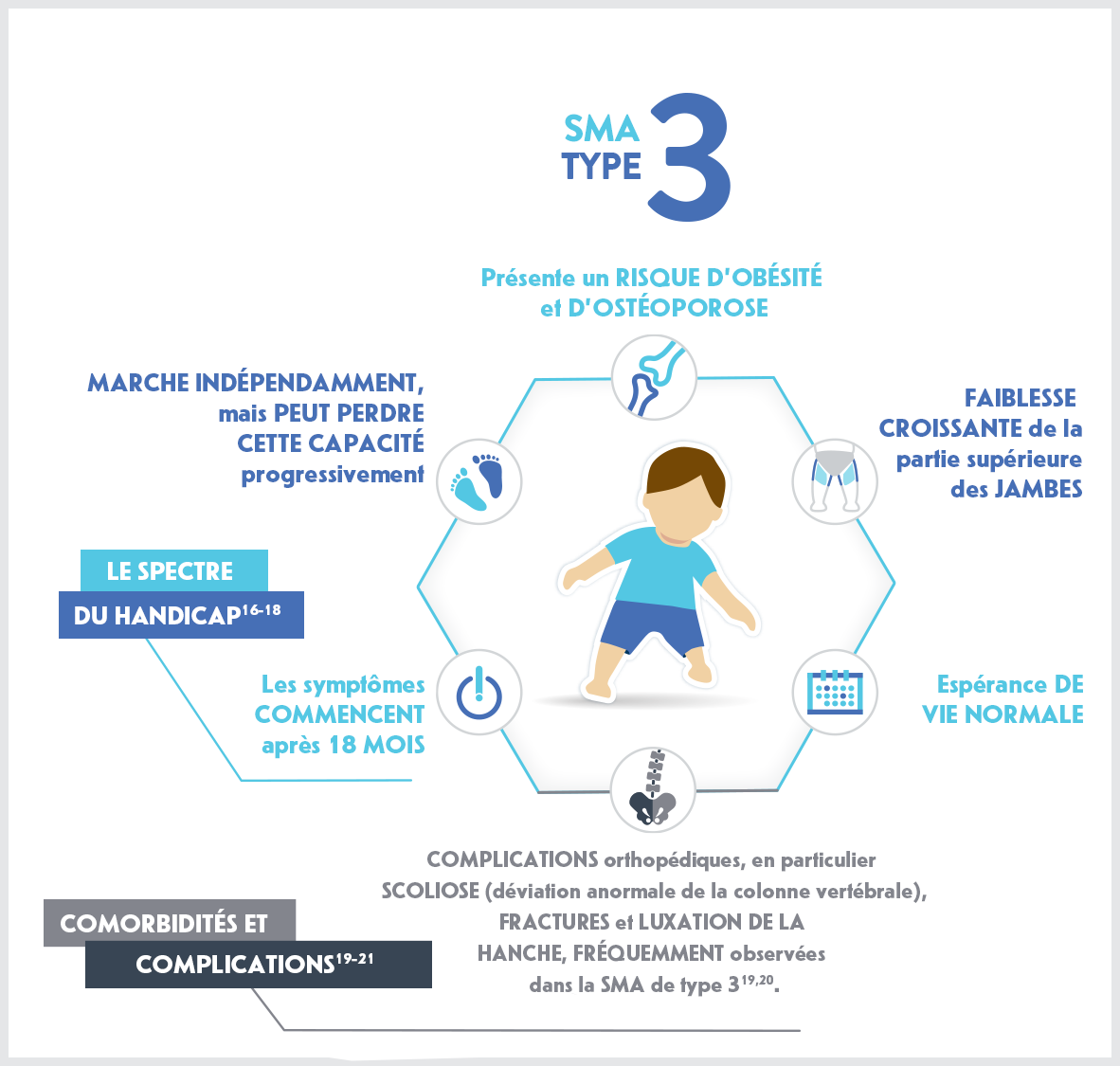
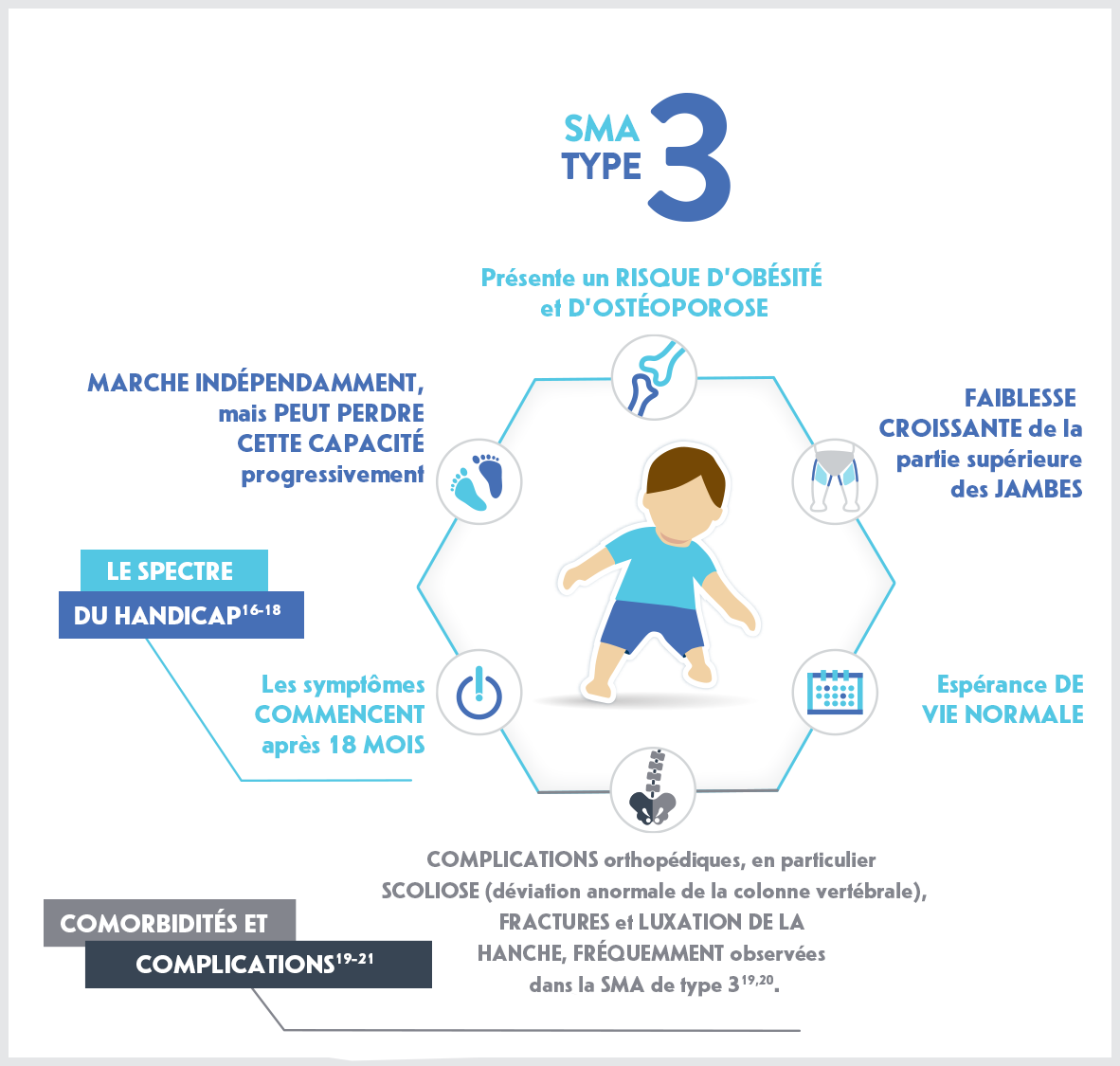
Caractéristiques1,5
- Scoliose
- Problèmes de déglutition et de mastication
- Les muscles des jambes sont généralement plus sévèrement affectés que les bras
- Douleur musculaire
- Symptômes de surmenage articulaire
- Risque d'osthéoporose quand le patient devient plus âgé
Progrès moteur le plus avancé
TOUT
Espérance de vie
NORMALE
Type
Type IV
Caractéristiques1,5
Les symptômes physiques sont similaires à ceux de l’amyotrophie spinale juvénile, avec l’apparition progressive de faiblesse, de tremblements et de contractions musculaires et sont initialement observés vers la fin de l’adolescence ou à l’âge adulte
L’amyotrophie spinale est souvent suspectée par un parent qui peut remarquer que son enfant n’atteint pas certains stades du développement moteur
Les parents peuvent remarquer que leur enfant n’atteint pas les étapes motrices typiques de son âge, comme la capacité à tenir sa tête droite, à faire une roulade ou à s’asseoir seul. La déglutition ou l’alimentation peuvent également devenir difficiles, et les enfants peuvent perdre la capacité à déglutir en toute sécurité sans s’étouffer ni inhaler les aliments dans les poumons (aspiration).9,13
Alors que tous les bébés se développent à leur propre rythme, l’Organisation Mondiale de la Santé (OMS) propose les directives générales suivantes concernant les étapes motrices, dans le cadre de l’Étude multicentrique sur la référence de croissance (Multicentre Growth Reference Study [MGRS]) :14
Progrès moteurs dans la MGRS
| STADE MOTEUR ATTEINT | CRITÈRES DE PERFORMANCE |
| S’asseoir sans aide | L’enfant s’assied droit avec la tête droite pendant plus de 10 secondes. N’utilise pas les bras ou les mains pour équilibrer le corps ou assurer la position assise. |
| Rampe sur les mains et les genoux | L’enfant se déplace vers l’avant ou vers l’arrière sur les mains et sur les genoux. Le ventre ne touche pas la surface de soutien. Mouvements continus et consécutifs, ≥ 3 d’affilée. |
| Se met debout sans assistance | L’enfant se tient debout sur les deux pieds, en se tenant à un support stable, comme un meuble. L’enfant se tient debout pendant ≥ 10 secondes. |
| Marche avec une assistance | L’enfant est en position verticale, le dos droit. Fait des mouvements latéraux ou vers l’avant, en se tenant à un support stable avec une main ou les deux. Une jambe avance tandis que l’autre soutient le poids du corps. L’enfant fait ≥ 5 pas. |
| Se met debout seul | L’enfant tient debout sur les deux pieds (mais pas sur la pointe des pieds), le dos droit. Les jambes soutiennent 100 % du poids, sans se tenir pendant ≥ 10 secondes. |
| Marche seul | L’enfant fait ≥ 5 pas seul, avec le dos droit. Une jambe avance tandis que l’autre soutient la majorité du poids. Il n’y a aucun contact avec une personne ou un objet. |
Adapté de l’Étude multicentrique sur la référence de croissance établie par l’OMS.14
| ÂGE DE L’ENFANT | MOUVEMENTS / ÉTAPES PHYSIQUES TYPIQUES |
| 2 mois |
|
| 4 mois |
|
| 6 mois |
|
| 9 mois |
|
| 1 an |
|
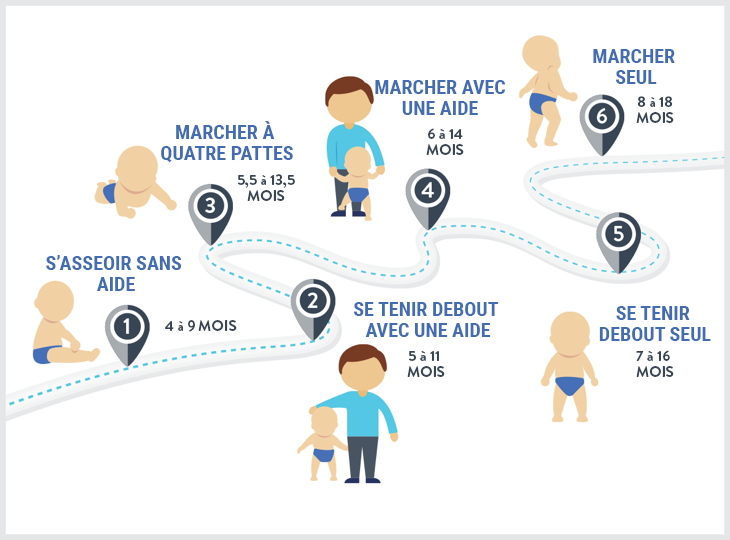

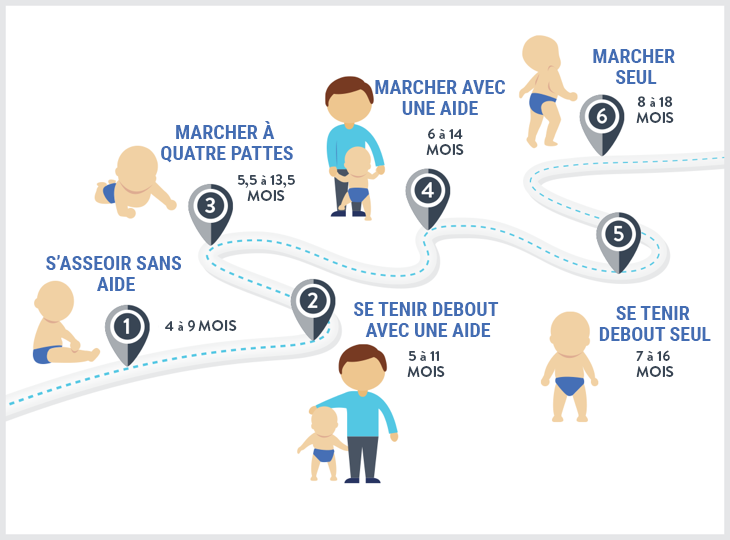
Adapté selon la la liste de contrôle des étapes établie par les Centres américains pour le contrôle et la prévention des maladies (Centers for Disease Control and Prevention).13



Les rapports des parents concernant le développement moteur global de leur enfant sont généralement fiables. Le fait de communiquer au médecin des observations sur les retards moteurs possibles peut aider à établir une stratégie appropriée.2,15
CONNECTEZ-VOUS
pour savoir comment rejoindre la communauté SMA
Les personnages présentés sont de vrais patients et le consentement requis pour utiliser leurs histoires a été obtenu auprès des patients et de leurs familles. Les photographies sont à titre d'illustration uniquement.
Références
1.Mercuri E, et al. Diagnosis and management of spinal muscular atrophy: Part 1: Recommendations for diagnosis, rehabilitation, orthopedic and nutritional care. Neuromuscl Disord. 2018;28(2):103-115.
2.Noritz GH, Murphy NA; and Neuromuscular Screening Expert Panel. Motor delays: early identification and evaluation. Pediatrics. 2013;131(6):e2016-e2027.
3.Kolb SJ, Kissel JT. Spinal muscular atrophy. Arch Neurol. 2011;68(8):979-984.
4.Markowitz JA, Singh P, Darras BT. Spinal muscular atrophy: a clinical and research update. Pediatr Neurol. 2012;46(1):1-12.
5.Prior TW, Russman BS. Spinal muscular atrophy. NCBI Bookshelf Website. Disponible sur : http://www.ncbi.nlm.nih.gov/books/NBK1352/. Mise à jour le 14 novembre 2013. Consulté le 15 avril 2016.
6.Iannaccone ST. Modern management of spinal muscular atrophy. J Child Neurol. 2007;22(8):974-978.
7.Oskoui M, Levy G, Garland CJ, et al. The changing natural history of spinal muscular atrophy type 1. Neurology. 2007;69(20):1931-1936.
8.Darras BT, Royden Jones H Jr, Ryan MM, De Vivo DC, eds. Neuromuscular Disorders of Infancy, Childhood, and Adolescence: A Clinician’s Approach. 2nd Ed. London, UK: Elsevier; 2015.
9.Cure SMA. Understanding Spinal Muscular Atrophy (SMA). Available at: https://www.curesma.org/wp-content/uploads/2020/08/08262020_Understanding_SMA_vWeb.pdf. August 2020.
10.Online Mendelian Inheritance in Man. Neuronopathy, distal hereditary motor, type VA; HMN5A. http://www.omim.org/entry/600794. Modifié le 2 janvier 2014. Consulté le 22 avril 2016.
11.National Organization for Rare Diseases. Spinal muscular atrophy. https://rarediseases.org/rare-diseases/spinal-muscular-atrophy/. Mise à jour 2012. Consulté le 17 avril 2016.
12.Barkhaus PE et al. Kennedy Disease. Disponible sur : http://emedicine.medscape.com/article/1172604-overview. Mise à jour : 8 juin 2016. Consulté le 9 janvier 2017.
13.Centers for Disease Control and Prevention. Developmental milestones. Disponible sur : http://www.cdc.gov/ncbddd/actearly/milestones/. Mis à jour le 21 janvier 2016. Consulté le 27 avril 2016.
14.Wijnhoven TMA, de Onis M, Onyango AE, et al; for the WHO Multicentre Growth Reference Study Group. Assessment of gross motor development in the WHO Multricentre Growth Reference Study. Food Nutr Bull. 2004;25(1 suppl 1):S37-S45.
15.Lawton S, Hickerton C, Archibald AD, McClaren BJ, Metcalfe SA. A mixed methods exploration of families’ experiences of the diagnosis of childhood spinal muscular atrophy. Eur J Hum Genet. 2015;23(5):575-580.
16.Kolb SJ, Kissel JT. Neurol Clin.. 2015;33:831-46.
17.D'Amico A, et al. Orphanet J Rare Dis. 2011;6:71.
18.Lunn MR, Wang CH. Lancet. 2008;371:2120-33.
19.Haaker G, Fujak A. Appl Clin Genet. 2013;6:113-20.
20.Darras BT. Paediatr Clin North Am. 2015;62:743-66.
21.Wang CH, et al. J Child Neurol. 2007;22:1027-49.
Code de travail: Biogen-240357 – juin 2024







































